Tvorba glykogenu
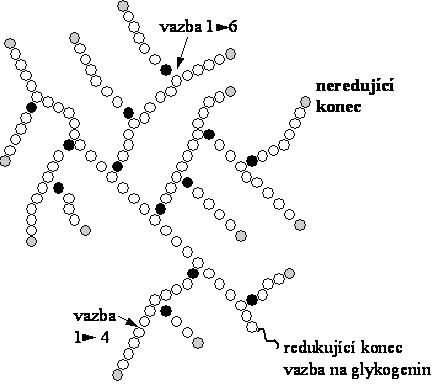
Glykogen je polysacharid s vysoce větvenou strukturou na bázi glukosy. Základ tvoří 10ti až 18ti-členné a-D-glukopyranosové zbytky s a[1 ® 4]-glykosidickými vazbami s větvemi, oddělujícími se od tohoto základu prostřednictvím a [1 ® 6]-glykosidických vazeb.
Struktura glykogenu:
Je hlavní zásobní formou sacharidů u člověka ve většině buněk; uvolňuje se z něho pro energetický metabolismus tkání tak potřebná glukosa. Jaterní glykogen (až 6% hmotnostního podílu), který slouží i jako zásoba glukosy pro udržovaní hladiny krevního cukru, je vyčerpán kompletně za 12 - 18 hodin hladovění; svalový glykogen (nejvýše 1% hmotnosti, ale co do celkového obsahu v těle 3-4 krát více než jaterní) je vyčerpán pouze po velmi těžké a prolongované tělesné námaze. Uspořádání molekuly do bohatého větvení umožňuje jeho velmi rychlé odbourání na glukosové jednotky.
BIOSYNTÉZA
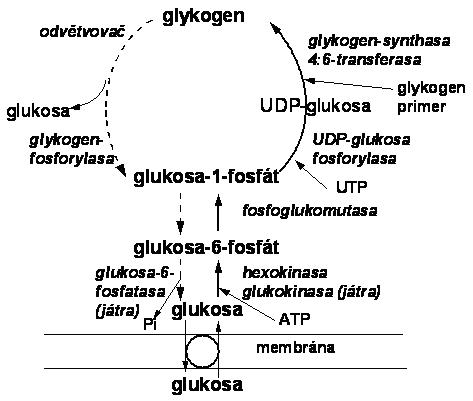
Syntéza a degradace glykogenu v játrech je regulována hormonálním mechanismem, jehož hlavním signálem je hladina glukosy- Glukosa je v hepatocytech fosforylována na glukosa-6-fosfát za účasti glukokinasy (ve svalech a jiných tkáních je to hexokinasa). Glukosa-6-fosfát se mění působením fosfoglukomutasy na glukosa-1-fosfát. Dalším krokem je reakce s uridintrifosfátem za vzniku aktivního nukleotidu uridindifosfát-glukosy (za katalýzy UDP-Glu-pyrofosforylasy). Působením enzymu glykogensyntasy dochází ke glykosidické vazbě mezi uhlíky C1 a C4 aktivního nukleotidu (UDP-Glu). Tímto způsobem se tvoří skelet polysacharidu; podmínkou je přítomnost malého množství "glykogenového primeru". Přidáním dalších glykosylových zbytků z UDP-glukosy se řetězec prodlužuje až vznikne řetězec o 11 zbytcích. Z něho se odštěpí amylo-4:6-transferasou 6–8 zbytků, které se znovu napojí vazbou a-1,6 jako postranní větev. Větvení řetězů 1 ® 6 glykosidickou vazbou se děje pomocí větvícího enzymu. (amylo [1 ® 4] ® [1 ® 6]-transglukosidasy).
ODBOURÁVÁNÍ
Není to "obrácená" glykogenogeneze, ale samostatná metabolická dráha, katalyzovaná dvěma enzymy: glykogenfosforylasou a odvětvujícím enzymem. Štěpení začíná s glykogenfosforylasou, která je limitujícím enzymem glykogenolýzy. Při této fosforolýze se štěpí vazba 1 ® 4 a odštěpuje se glukosa-1-fosfát. Takto se odbourávají glukosové jednotky až zůstane čtyřglukosový zbytek řetězce. Enzym a-[1 ®4] ® a-[1 ® 4] glukantransferasa přenáší trisacharidovou jednotku z jedné větve na druhou vystavujíc přitom místo [1 ® 6]-glykosidické vazby hydrolytickému účinku. Hydrolýza této vazby se děje za katalýzy odvětvovacího enzymu - amylo-[1®6]-glukosidasy. Po odstranění postranní větve může pokračovat působení fosforylasy.
REGULACE TVORBY GLYKOGENU
Regulace syntézy glykogenu v různých tkáních se řídí funkcí glykogenu v některé tkáni. Jaterní glykogen slouží hlavně jako zdroj glukosy cirkulující v krvi, která je v době hladovění nutná pro energetický metabolismus buněk, které ji využívají výlučně nebo v době nedostatku z vlastních zdrojů. Regulace je uskutečňována podle poměru insulin/glukagon a dle hodnoty glykemie. Degradace jaterního glykogenu je spouštěna též působením adrenalinu, který je uvolňován z dřeně nadledvinek při fyzické zátěži, při hypoglykemii apod. Naproti tomu svalový glykogen slouží jako zásoba glykosylových jednotek vstupujících do glykolytické dráhy, aby poskytla energii pro regeneraci ATP při svalové práci. Koncentrace AMP je signálem nedostatku ATP ve svalové buňce a je spouštěcím signálem svalové glykogenolýzy. Rovněž adrenalin uvolňovaný za stresových situacích navozuje glykogenolýzu ve svalech.
cAMP sdružuje regulaci glykogenolýzy a glykogenogeneze, a to prostřednictvím glykogenfosforylasy, a to jak alosterickým mechanismem, tak kovalentní modifikací navozenou reversibilní fosforylací a defosforylací enzymového proteinu. Fosforylasa jaterní a svalová se liší jak imunologicky, tak geneticky. Fosforylasa svalová je aktivována adrenalinem prostřednictvím cAMP-dependentní proteinové kinasy (fosforylací inaktivní fosforylasy b na aktivní fosforylasu a). Ca2+ synchronizuje aktivaci fosforylasy se svalovou kontrakcí. Glykogenolýza ve svalech tímto mechanismem po svalové kontrakci stoupá až několiksetkrát. Důležitou roli hraje přitom kalmodulin. Glykogenolýza v játrech může probíhat též bez závislosti na cAMP. Bylo totiž zjištěno, že kromě tvorby cAMP po vyplavení (podání) glukagonu dochází také k aktivaci fosforylasy v játrech prostřednictvím a1-receptorů; z nich nastartovaný" chemický" signál se uplatní prostřednictvím uvolnění Ca2+ z mitochondrií
a jejich toku do cytosolu, kde je tak vyvolána aktivace kalmodulin-senzitivní fosforylasy.
Regulace glykogenového metabolismu je výrazem vyvážené aktivity mezi glykogensynthasou na jedné straně a fosforylasou na straně druhé.